同じ言葉なのに
「殺される文」と
「生き残る文」がある
私たちの体の設計図はDNAに書かれています。
DNAは約30億文字からなる巨大な
「レシピ本」のようなもので、
そこには約2万種類のタンパク質
(体を動かす部品)の作り方が書かれています。
でも、
DNAは直接タンパク質を
作るわけではありません。
工事現場で例えると、
DNAは「金庫に保管された
工場全体の設計図」で、
各細胞の核に保管された貴重品です。
そんな貴重品を部品を組み立てるごとに
引っ張り出すのは、かなりのリスクです。
そこで私たちの細胞は大元の設計図ではなく、
一部をコピーした「設計図の部分写し」として
mRNAという分子を使用します。
人間の大工さんなら、
この部分写しとにらめっこしながら、
木材を切り出し、形を整え、
担当する区画を構築していきますが、
細胞はもう少しオートマチックです。
設計図の部分写し(mRNA)を
部品自動組み立てマシーン
(リボソーム)に差し込むだけで、
組み立てマシーンが設計図の
情報を読み取りつつ、
しかも材料であるアミノ酸をどんどん
取り込みながら次々に繋げて、
タンパク質を作ってくれます。
ではどうやって情報を読み取っているかというと、
基本にあるのは3文字セットのコードです。
たとえば「GCT」という3文字セットが
あればそれは「アラニン」という
アミノ酸を指定することになります。
DNAの暗号は4種類の文字が
長く長く繋がっていますが、
タンパク質の情報が書かれている部分は、
基本的にこの3文字セットが
延々と続く形で情報が記述されています。
人間の体を作るのに使われている
アミノ酸は20種類あります。
「A・T・G・C」の1文字が1つのアミノ酸に
対応しているだけなら、
4種類のアミノ酸しか使えません。
そこで文字を組み合わせて、
複数のアミノ酸を指定できるようにしているわけです。
しかし問題はここからです。
4種類の文字を3つ並べる組み合わせは
4×4×4で合計64通りあります。
このうち3つは
「ここで翻訳終了」を意味する
終止コドンなので、
アミノ酸を指定するのに使えるのは61個です。
これで20種類のアミノ酸を指定すればいいので、
41個分が「余ってしまう」わけです。
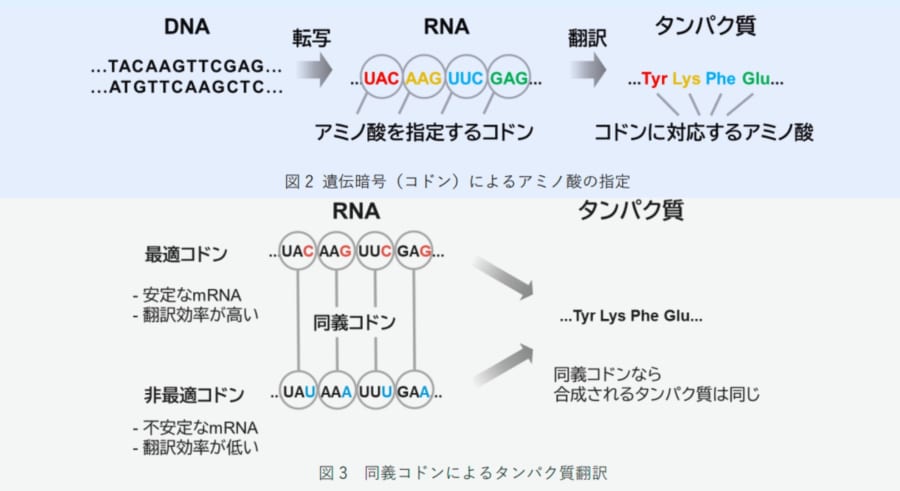
そこで生命はダブりを許可しました。
先ほど「GCT」がアラニンに対応すると言いましたが、
実はアラニンを指定するコドンは
「GCT」の他に「GCC」「GCA」「GCG」
とあわせて4種類も存在しているのです。
英語で「look」「see」「watch」がどれも
「見る」というニュアンスになるように、
「GCT」「GCC」「GCA」「GCG」は
スペルが違ってもどれもアラニンという
アミノ酸を持ってこいという指示になるわけです。
生物学者たちはこれを長らく
「ただの冗長性(あそび)にすぎない」と
考えていました。
教科書でもこう教えます――
「どのスペルを使っても、
作られるタンパク質は全く同じ」と。
ところが以前から、
どれを選ぶかで遺伝子の活発さが
大きく変わることが観察されるようになりました。
特にヒトの細胞ではGやCで終わる
コドンを使うと遺伝子は活発に働き、
AやUで終わるコドンを多用すると、
なぜかその遺伝子の部分写し
(mRNA)が作られても早々に分解されてしまい、
結果としてタンパク質がほとんど作られないのです。
「意味が同じコドンなのに、
なぜ結果が違うのか」
これがヒト細胞において長年解けない
謎として残っていました。
受付をしているやさしい
オジサンが殺し屋への通報役だった
「DNAには第2のコード」が存在すると判明
遺伝子を密かに黙らせる隠し指令機構の正体
京都大学の竹内理氏、吉永正憲氏、
理化学研究所の伊藤拓宏氏らのチームは、
この犯人探しに容赦ない手段で挑みました。
ヒトの全遺伝子を一つずつ潰し、
「どれを潰したら不良品mRNAが生き
延びるようになるか」を片っ端から試したのです。
すると、
浮かび上がったのは、まさかの「受付係」でした。
先に述べたようにDNAの情報はいったん
「mRNA」にコピーされます。
そのコピー用紙を「リボソーム」という
製造機械が読み取り、
アミノ酸を順番につなげて
タンパク質を完成させます。
今回主役となるDHX29は、
これまで「この組み立てマシーンに設計図を
セットする受付係」だと思われていました。
具体的に言うと、
mRNAという設計図の写しには、
たまに折れ曲がったり絡まったりした
「くせ字」の部分があります。
そのままではマシーンが差込口から
読み込めないので、
DHX29がそのしわを伸ばし、
マシーンの読み取り開始位置まで
mRNAを正しくセットしてあげる
そんな工場入り口の受付兼セッティング係というのが、
2008年以来ずっと彼に与えられていた肩書きでした。
ここまではよくいる親切なオジサンの話ですが、
今回の研究で彼にはもう一つ、
誰も知らなかった顔があったことが発覚します。
話を進める前に、
もう一度あの謎を思い出してください。
ヒトの細胞では、
GやCで終わるコドン(優等生スペル)で
書かれた設計図はタンパク質を
ちゃんと作れるのに対し、
AやUで終わるコドン(劣等生スペル)ばかりで
書かれた設計図は、
なぜかタンパク質がほとんど
作られないという現象がありました。
この差を素直に説明しようとすれば、
こういうイメージになります。
優等生スペルの区間では、
材料であるアミノ酸を運ぶ配送トラック
(tRNA)が高速で搬入口に到着するので
ライン作業がサクサク進む。
一方、
劣等生スペルの区間では、
読みにくさのせいでトラックの到着が少し遅れ、
ライン作業が鈍る。
しかしこれはあくまで製造速度の話で、
本来なら少し遅れるだけで済むはずです。
ところが現実の細胞では、
劣等生スペルを多く含む設計図は
「少し遅れる」どころか、
製造が完全に止まり、
しかも設計図自体まで消えてしまうことがあります。
まるでAやUで終わるコドンの多い部分設計図
(mRNA)を狙う処刑人がいて、
抹殺しているかのようです。
では、その処刑人は誰なのか。
ここで、
今回の研究で顕微鏡が捉えた
衝撃の光景に戻ります。
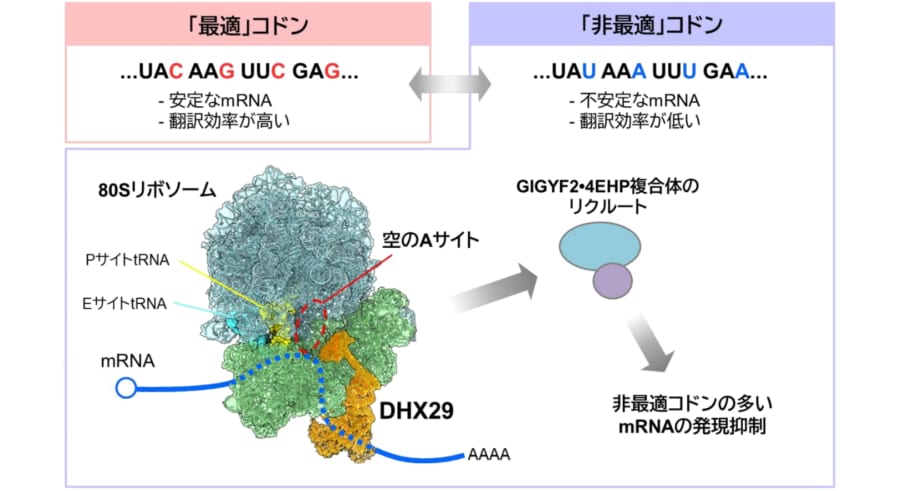
リボソームの搬入口を覗いてみると、
そこには「受付のやさしいオジサン」
だったはずのDHX29が、
堂々とアミノ酸を積んだトラックの
「搬入口」居座っていたのです。
しかも彼が座り込むのは、
ただの巡回ではありませんでした。
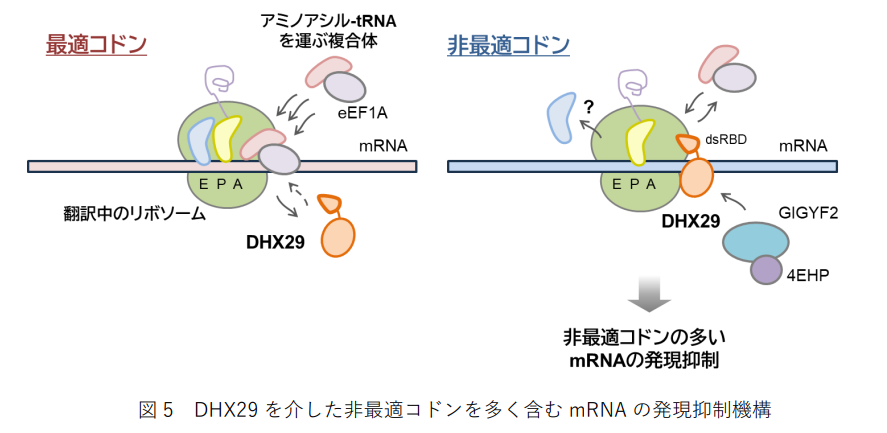
優等生スペルの区間では、
配送トラックが途切れなく到着し続けるので、
DHX29は搬入口に割り込むことはありません。
ところが劣等生スペルの区間では、
トラックの到着が鈍ります。
その「空いた一瞬」をDHX29は見逃しません。
ぽっかり空いた搬入口に、
すっと自分が腰を下ろしてしまうのです。
ここからが処刑の始まりです。
搬入口に陣取ったDHX29は、
次に電話を一本かけます。
呼び出されるのは
GIGYF2・4EHP複合体という執行班。
彼らはmRNAのてっぺんにある
「キャップ」と呼ばれる構造にフタをかぶせて
組み立てマシーンの稼働を止め、
設計図そのものを分解装置へと
容赦なく送り込むのです。
つまりDHX29は、
スペルを直接読んで優劣を
判定しているわけではありません。
「搬入口がなかなか埋まらない」という
サインを嗅ぎつけて、
その設計図が劣等生スペルだらけであることを
間接的に見抜いていた、というわけです。
やや映画チックに言うなら、
受付のやさしいオジサンだと思っていた人
(DHX29)が、
配送トラックが遅れて入り口が空いた瞬間――
つまり劣等生(AやUで終わるコドン)が
並んでいると気づいた瞬間――
に入り口をふさぎ、
処刑人(GIGYF2・4EHP複合体)を呼び
寄せ劣等生の頭に袋をかぶせて
分解装置に投げ込むというわけです。
こうして劣等生スペルで書かれた
設計図の写しは、
誰にも気づかれないまま、
静かに破棄されていたのでした。
酵母のような単純な生物では以前から
別系統の処刑人が知られていましたが、
ヒト細胞でそれと異なる新しい
mRNAの処刑機構が見つかったことには
大きな意味があります。
それは次ページで紹介する
「mRNAワクチンの効果アップ」や
「がん治療」さらに「自己免疫疾患の治療」に
もかかわる発見になり得るからです。
この発見は、
基礎生物学の教科書を書き換える
だけにとどまりません。
私たちの未来の医療までも、
静かに、しかし根本から変えてしまう
可能性を秘めているのです。
まず最も直接的な影響を受けるのが、
mRNAワクチンとmRNA医薬品の分野でしょう。
新型コロナウイルス禍で世界を救った
あの技術の本質は、
人工的に作った
mRNA(タンパク質の設計図の写し)を
体に注射し、
体内でウイルスの目印を作らせて
免疫を訓練する、というものでした。
この方法で効き目を決める大きな要素の一つは、
注射されたmRNAが体の中でどれだけ
長く生き延びられるかです。
必要とするmRNAの設計図のコドンにAやUが多いと、
体内ですぐに分解されてしまい、
十分な量の目印タンパク質が作られないまま、
治療効果が尻すぼみに終わってしまいます。
ですが今回の発見を応用すれば話は変わります。
将来的には、
DHX29の目をかいくぐりやすいスペル
(優等生コドンばかりを集めた設計)で
mRNAを書き直せば、
少ない投与量でより長く効く
ワクチンや薬が作れるかもしれません。
これは現在、
世界中の製薬会社が火花を散らしている
mRNA医薬品開発レースの、
ルール自体を書き換えかねない知見です。
次に期待されるのが、
がん治療への応用です。
実はDHX29遺伝子に異常が
見つかるがんの報告が、
一部で出てきていました。
mRNAの品質管理が壊れることで、
本来なら処分されるべき不良設計図の
タンパク質が増えてしまい、
それが細胞のがん化を後押ししている
可能性がある
そんなシナリオが、
今回の発見で現実味を帯びてきたのです。
この場合、
もし何らかの手段でDHX29の
機能を回復してやれば、
遺伝子チェックが正常に戻り、
がん化を押しとどめたり、
がん細胞の増殖にブレーキを
かけたりできるかもしれません。
さらにこのメカニズムの異常は、
自己免疫疾患や神経変性疾患にまで
顔を出し始めています。
「不良設計図のmRNA」が処刑を免れて
細胞内に残り続けると、
そこから余計なタンパク質が過剰に作られ、
免疫系が自分の細胞を攻撃する引き金になったり、
神経細胞の中に異常なタンパク質が蓄積して
神経を壊してしまったりすると考えられるからです。
つまりDHX29は、
一つの病気の原因というよりも、
多くの難病を横断する「共通の急所」の
有力な候補として浮上したわけです。
この共通の急所を狙い撃ちできる薬が作れれば、
複数の病気に一気に効く治療薬が
生まれる可能性さえあります。
同じ意味のはずのスペルに、
命の設計図の寿命を決める隠された意味があった・・・
そしてその意味を読み取る番人は、
あなたの細胞のなかで今この瞬間も、
音もなく空いた席を探して歩き回っている。
日本主導の国際チームが
引きずり出したこの事実は、
生命がいかに繊細で、
多重で、
そして私たちの理解よりずっと巧妙に
設計されているかを、
教えてくれました。
<参考: >